
宏基因组测序技术作为近年来在临床感染领域的明星技术,近三年来,全国各单位和专家陆续编写发表多篇宏基因组技术应用于感染疾病诊断的专家共识[1-4],推进了宏基因组技术在临床的应用和普及,提高NGS技术应用于感染性疾病病原诊断的质量。梳理宏基因组测序技术应用变迁脉络,以更宽的视角看待宏基因组测序技术发展中的机遇和挑战,展望未来,推动mNGS技术更高效、更安全、更标准地应用于临床。
mNGS技术作为病原诊断“新事物”,对于临床适应证的选择,一直以来受到行业专家关注,在近几年大致经过了萌芽期、上升期、发展期和扩张期四个阶段。在早期专家共识中,推荐在感染周期的后期、危急重症或者常规病原检测无效的时候,送检mNGS。相信这是由于mNGS刚应用于感染病原诊断,临床上对于mNGS特性还掌握不深,只有在传统诊断方法束手无策时才考虑送检mNGS。 但随着mNGS在临床上的广泛应用,临床专家对于mNGS技术更加了解,并积累下大样本数据,并将应用时机在感染周期中前置。因此,在近期的专家共识中指出,除了在危急重症中使用mNGS之外,临床判断发生疑似感染,即可使用mNGS辅助诊断,不再刻意区分轻重症,早送检,争取治疗时机。随着mNGS相关应用指南或专家共识的陆续发表,临床适应证范围也越来越大,梳理其发展路径,在最新的专家共识中指出可以看出,除了在危急重症、中危重以及临床明确疑似感染中推荐mNGS外,还专门新增了慢性感染、流行病学和感染控制这两部分内容。随着新冠疫情的发生,以及慢性感染发生率逐年上升,mNGS的检测优势与临床价值更加凸显。这也和部分专家认为mNGS可以在慢性感染、微生物学、耐药学、流行病学和感染控制等方面可以发挥更大价值的观点一致。相信随着临床更大样本量的验证,新的临床适应证会得到进一步验证和细化,也许有一天,mNGS检测技术可以更加广泛甚至可以普及,给临床感染疾病诊断带来更加明确的参考证据,造福更多患者。我们也期待这一天尽早到来。
无论是何种诊断技术,要获得准确的检测结果,合符规则和标准的样本采集是重中之重。 整理近年来多篇专家共识,对于样本选择,专家作出了如下建议: 
一致认可观点: 1、从正常无菌部位采集 mNGS 检测标本,应严格无菌操作,避免污染。从有菌定植或污染部位采集的标本,应采取必要措施,尽量减少污染; 2、多篇专家共识共同提到,应尽量送检感染部位的体液或者组织标本,以提高检测结果的可信度,只有在不易采集或者标本不理想时,可选择外周血液标本,但有可能会降低检测结果的准确性; 或存争议观点: 1、标本选择上,早期专家共识考虑到定植菌群会增加后期结果判读难度等原因,推荐尽量送检无菌部分的标本,以获得更大的临床价值。而近期的专家则放开选择范围,从有菌定植或污染部位采集的标本,在采取必要措施,尽量减少污染的情况下,亦可送检; 2、在最新一篇专家共识中着重指出,用于宏基因组 RNA 测序的标本,应添加核酸稳定剂,保证标本质量。 我们可以看到,专家共识一直以来对于样本采集的要求都是严格的,一丝的采样不严谨有可能在灵敏的mNGS检测中被无限放大,这在多篇专家共识中已多次强调。在标本选择上,专家们对于定植菌群是否会对后期结果判读产生阻碍存在分歧,对于是否可以从有菌定植或污染部位采集标本暂未达成一致共识。而对于核酸稳定剂应否添加,行业内也出现不同的声音,有学者认为标本中添加核酸稳定剂有可能损伤病原核酸,影响检测质量。因此,专家共识当中依然有不少观点存在分歧,还需要行业进行更多研究来验证和探讨。
mNGS检测流程在多篇专家共识中大致相同,遵循标本采集、核酸处理、文库构建、测序、生物信息分析等流程。在多篇专家共识中,都对检测流程中的质量控制加以强调,并作出更加细致的要求,认为建立科学完善的质量控制指标和体系,对于检测结果的质量至关重要。另外,在最新专家共识中,特别强调了去宿主这一步骤,认为去除宿主细胞或核酸,可以增强高背景标本的mNGS检测灵敏度。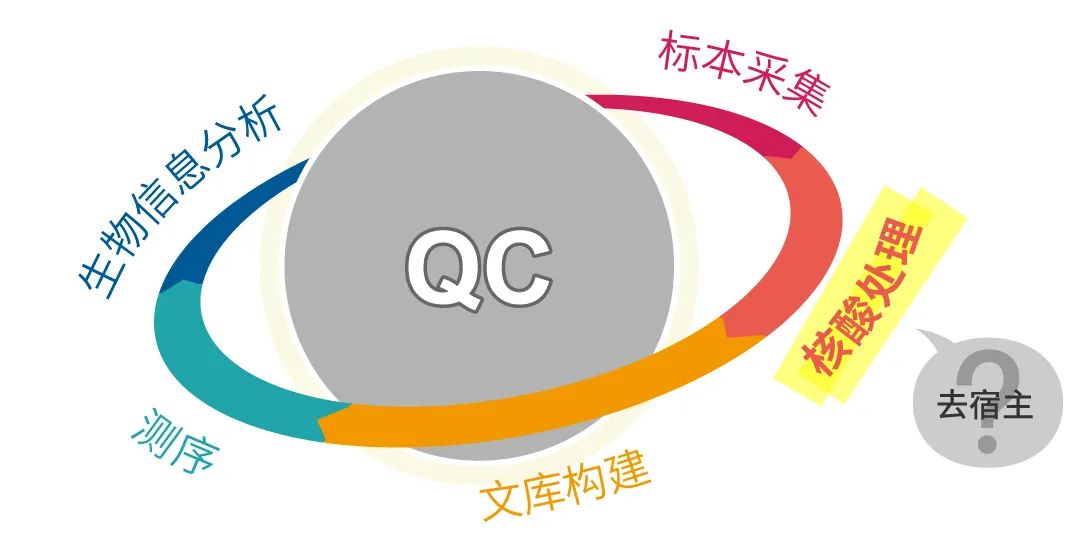 最新的共识中,首次对去宿主问题进行了全面的阐述,明确了对于高宿主背景标本提取时应采用经过验证的方法去除宿主细胞或核酸,以提高检测的灵敏度。高背景主要来自人类宿主(例如组织活检标本)或微生物菌群(例如呼吸道标本、粪便等),如在临床样本中通常含有大量人体细胞和核酸,而病原含量很少(低于1%),在这种情况下,不改变mNGS检测策略(如测序数据量等),同时有效的去除样本背景,对于增加检测的准确性、灵敏性,和降低检测成本均具有重要作用。 在对于去宿主这个问题上,行业上也有不同的声音,认为在去宿主带来样本中有效测序数据显著提高的同时,也需要考虑技术体系不成熟导至的这一处理过程对病原微生物核酸的损失风险。也就是说如何高效去除样本背景,有效富集病原核酸,是考验这一实验过程是否能够应用临床检测的关键。而对于这一风险评估需要更多的研究来支持。相信随着mNGS技术的发展,可以很好解决高背景标本检测难题,提高mNGS技术应用于感染性疾病病原诊断的质量,为临床抗感染诊治能力提升提供帮助。目前去宿主的方法有:试剂盒法(如蛋白结合甲基化核酸),过滤法(如过滤膜/器)、yPMA(渗透裂解细胞后用叠氮碘化丙锭处理)、靶向杂交法等多种方法,去除效率差异较大,整体去除效率在9%~91%,如下方文献[5]图中提到的PMA去除效率最好,不同的文章中对此也存在不同的看法。 Raw:未过滤宿主,5种去宿主方法:分别为Fil(5-μm滤膜过滤)、NEB(1种试剂盒)、Mol(1种试剂盒)、QIA(1种试剂盒)、 lyPMA(渗透裂解细胞后用叠氮碘化丙锭处理)临床样本复杂,除了自身携带背景之外,也有被污染可能,同时mNGS检测流程中使用的试剂也存在背景问题,且操作环节较多,如何有效地避免污染是共识中反复提到的观点,也给出明确指导原则,但是这个问题只能尽量减少,不可能完全避免。那么最终所有环节的背景均会通过检测结果显示出来,如何有效鉴别/避免因污染而导至的结果误读也是需要特别关注的内容。共识中明确提出了几个观点: 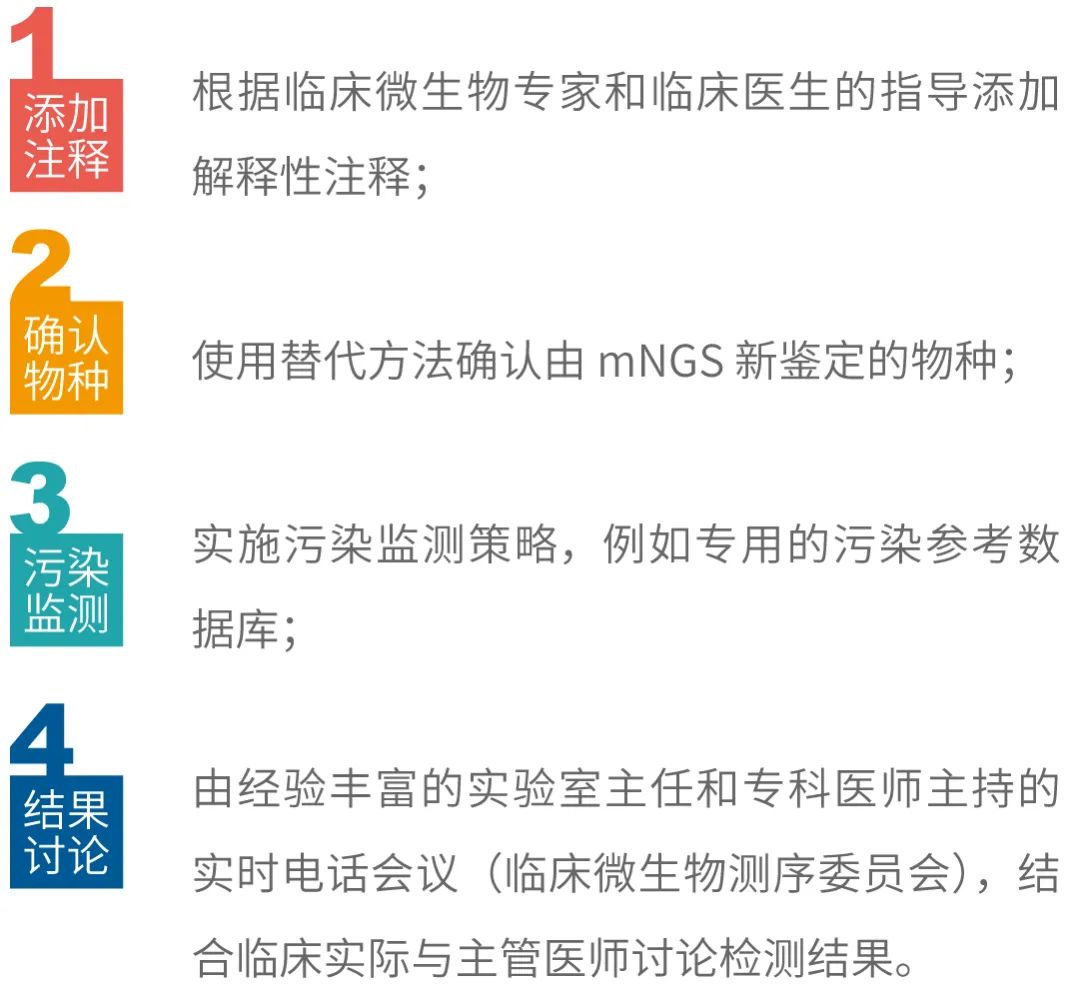
除此之外,小编还想进一步补充自己的观点,实验室深度清洁可以从根本上有效减少实验环境中的气溶胶给实验造成的污染,同时也可以降低检测报告中的病原体判定难度。
临床感染病原学诊断是具有挑战性的工作,mNGS仅检测样本中的核酸,与传统病原诊断有所区别,行业需要对mNGS报告有更深刻的了解,才能使mNGS更好地服务于临床。而随着mNGS不断应用于临床,在最新的专家共识中,mNGS报告的解读规则已逐渐明确清晰: 1、解读报告考虑如下参数:测序质量、读长、特异性读长、覆盖率、深度、丰度、微生物序列的数据量、阈值等; 2、mNGS 检测报告中,建议结合不同标本类型与检出病原微生物的种类进行解读,区分无菌部位与正常有菌部位。确认致病微生物时,应考虑检出微生物是否为感染部位的潜在病原。注意排除常见定植菌、污染菌与工程菌的影响; 3、血浆样本对 cfDNA 进行 mNGS 检测时,建议从临床的角度鉴别检出序列属于致病微生物、样本污染、死亡微生物裂解,还是定植菌群所致的一过性菌血症;4、mNGS 报告中常规容易培养的病原菌,建议临床医师结合传统方法,综合判断其临床价值;5、建议对于在核酸提取过程中破壁困难的微生物,即使在检测报告中读长数较低,也要考虑其为致病微生物的可能,并采用其他方法验证;6、采用 mNGS 进行病原微生物鉴定的同时,可以考虑检测耐药基因,但需要将耐药基因准确定位到具体的病原体上以明确其临床价值;7、建议解读报告单前应了解比对数据库的内容,明确其是否涵盖少见病原或新发病原;8、mNGS 结果为阴性,对于排除感染常具有较好的阴性预测值。但对于某些病原微生物,如结核分枝杆菌等,原始样本中含量较少,或核酸提取困难的病原微生物,应考虑 mNGS 检测灵敏度较低,阴性预测性差,并不一定优于 PCR 等常规检测方案;9、建议各实验室建立自己的mNGS病原诊断阈值,并在临床工作中加以验证;10、不同病原微生物基因组大小不同,核酸提取效率存在差异,致病力也相去甚远,因此不能仅仅依靠读长多少来判断是否感染,建议同时考虑病原微生物种类差异与致病特性;11、mNGS病原微生物检测结果,建议由具有一定生物信息学知识,并从事临床感染或临床微生物等专业人员,结合患者临床背景、影像学资料、其他的实验室检查结果,综合判断,得到正确的解读与甄别。专家共识中列出了mNGS报告解读的各个指导原则,而在临床实际应用中,还有一些问题亟待解决,如检测耐药基因,还需要行业进行进一步研究和验证。mNGS测序是对病原体的全部核酸进行检测,也给耐药基因的检测提供了可能,也赋予更多检测希望,但是目前还存在诸多疑问需要解决。正如共识中提到的对于正常有菌部位样本,将耐药基因与特定病原微生物准确匹配存在较多困难。据文献报道,目前mNGS检测耐药基因与药敏一致性大约在40%左右,如何提高这一吻合度不仅是考验宏基因组检测,也同时挑战着临床耐药机制机理、临床耐药基因型与表型的大数据研究。说白了,就是需要先解决: 
而这一问题的解决,需要基因检测行业中的参与者,如医院医生、企业以及政府等方面共同支持,所以感染大数据及耐药大数据分析是迫切需要进行的。
结 语 行业上,mNGS应用于临床病原诊断从决策“用不用”,“怎么用”到“用得好、用得精准、用得有价值”发展。就像所有其他新技术一样,mNGS在临床上规范应用和正确解读报告数据方面仍然任重道远。随着技术的进一步成熟,二代测序病原体诊断标准完善,质量控制能力提升,同时增加大样本量的研究,最终建立中国感染病原体宏基因组学检测的标准规范,安全、理性地应用该技术,发挥更大价值,造福临床。
[1] 宏基因组分析和诊断技术在急危重症感染应用专家共识组. 宏基因组分析和诊断技术在急危重症感染应用的专家共识 [J] . 中华急诊医学杂志,2019,28 (2): 151-155. DOI: 10.3760/cma.j.issn.1671-0282.2019.02.005.[2] 宏基因组学测序技术在中重症感染中的临床应用共识专家组, 中国研究型医院学会脓毒症与休克专业委员会, 中国微生物学会微生物毒素专业委员会, 等. 宏基因组学测序技术在中重症感染中的临床应用专家共识(第一版) [J] . 中华危重病急救医学,2020,32 (05): 531-536. DOI: 10.3760/cma.j.cn121430-20200228-00095.[3] 《中华传染病杂志》编辑委员会. 中国宏基因组学第二代测序技术检测感染病原体的临床应用专家共识 [J] . 中华传染病杂志,2020,38 (11): 681-689. DOI: 10.3760/cma.j.cn311365-20200731-00732.[4] 中华医学会检验医学分会临床微生物学组, 中华医学会微生物学与免疫学分会临床微生物学组, 中国医疗保健国际交流促进会临床微生物与感染分会. 宏基因组高通量测序技术应用于感染性疾病病原检测中国专家共识 [J] . 中华检验医学杂志, 2021, 44(2): 107-120. DOI: 10.3760/cma.j.cn114452-20201026-00794.[5] Marotz CA, Sanders JG, Zuniga C, Zaramela LS, Knight R, Zengler K. Improving saliva shotgun metagenomics by chemical host DNA depletion. Microbiome. 2018 Feb 27;6(1):42. |  /3
/3 