无论您使用何种分子生物学技术,在某些时候,您都必须清理 DNA 样品,以去除珍贵样品中的缓冲液、污染物和核苷酸等物质,以便为下游实验提供完美纯净的 DNA。
磁珠是一种 DNA 纯化选择。它们简单而有效,而且它们令人放心的宏观性质对分子生物学家来说是一个可喜的变化!
但即使是这种看似简单的技术也可能出错,并提供次优的 DNA 最终产物。为了帮助确保 simple 保持有效,以下是我使用磁珠从 DNA 纯化中获得最佳结果的七个技巧: (1)不要冻结您的磁珠 永远不要冻结你的珠子。除非另有说明,否则磁化珠子永远不能被冻结。珠子应始终保持在 2 至 8ºC 的温度下。冷冻和解冻可能会导至珠子表面出现裂缝。这可能会导至样品污染 - 与您想要的相反。 (2)将微珠置于室温下 虽然您的磁珠应储存并保存在 2 至 8ºC 下,但您需要在使用前将其置于室温下。因此,请提前计划,并确保在需要珠子前 30 分钟将珠子从仓库中取出。这段时间将使珠子有时间预热。 (3)均质化您的磁珠 当您从仓库中取出珠子时,您很快就会意识到您的珠浆不均匀,颜色也不均匀。相反,您会在试管底部看到棕色珠子沉淀。随着分子生物学实验室的讨论,磁珠是巨大的!因此,它们在储存过程中会沉淀下来,这并不奇怪。但是,您需要均匀的珠浆,因此在使用珠子之前立即涡旋。确保对珠子进行涡旋,直到浆液呈均匀的颜色,并且所有珠子都处于悬浮状态。如果您的磁珠悬浮液不是均质的,则可能会危及您的方案;如果您继续使用相同的珠子,则您当前的 1 个或以下的 1 个。这是因为...... (4)您必须知道您的 DNA-Bead 比率 协议是有原因的,确切的数量很重要。磁珠起始量与您应该获得的 DNA 量直接相关。珠子太多,您可能会得到污染物。珠子太少,您可能会损失产品。因此,当您移液磁珠时,请务必清理掉挂在移液器吸头外侧的任何液滴。当然,请确保使用良好的移液规范,包括定期校准移液器。 (5)注意您的磁性支架 确保选择适合您所用产品的磁力架 - 无论您使用的是 8 联管、96 孔板还是 MIDI 板。洗涤方案通常包括许多“去除上清液并丢弃”的步骤。在这些步骤中丢失一些磁珠是正常的,但您希望尽量减少磁珠损失——当然,因为您的样品会附着在磁珠上!而且,我相信您和我一样担心在洗涤过程中丢失样品。因此,请使用合适的磁力架。除了尺寸之外,机架的磁铁位置也各不相同。磁体放置会影响磁珠的聚集位置 - 无论是在孔的底部、左侧、右侧还是呈环状构象。如果您的说明书没有指定哪个支架最好,您可以根据个人喜好进行选择。只需注意你正在使用的东西!您需要从聚集的磁珠中移出,以尽量减少意外吸走磁珠。并尝试找到具有良好磁强度的支架。 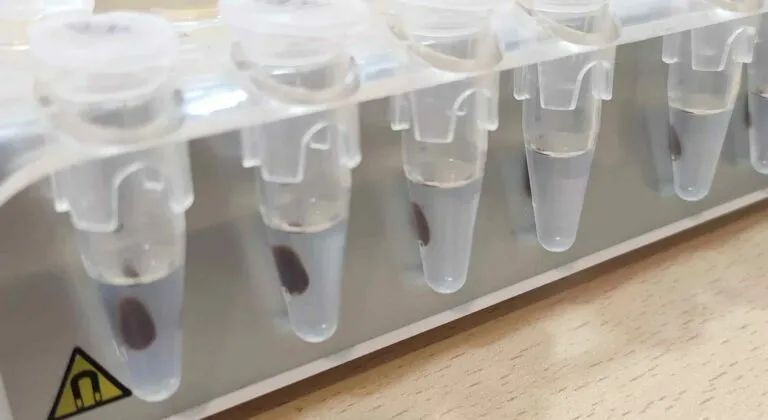
(6)小心移液 您当然知道这一点,但以下是我经验丰富的移液建议:吸液时:
保持手指稳定。现在不是匆忙的时候,也不是在拿铁咖啡中多喝一杯浓缩咖啡的日子。
不要吸气太快。慢慢来,因为吸液的强度可以克服磁力,并且您可以吸吮移液器吸头上的珠子。 (7)监控您的损失 如果您想知道您损失了多少磁珠(和样品),那么我建议您为每个样品保留一个“废液井”。换句话说,收集所有吸出的洗涤液。最后,您可以将这些废料很好地放在磁力架上,并实际查看每个洗涤步骤损失了多少珠子。这可以帮助您阐明为什么某些示例可能比其他示例效果更好。不是定性的,但仍然有帮助。如果您拥有良好的磁珠使用方法、稳定的手指和专注的眼睛,我保证您会将磁珠浪费降至最低,并增加纯化样品的保留率。洗涤快乐!
|  /3
/3 