金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
体外诊断(IVD,In-Vitro Diagnostics)是指将血液、体液、组织等样本从人体中取出,使用体外检测试剂、试剂盒、校准物、质控物等对样本进行检测与校验,以便对疾病进行预防、诊断、治疗检测、后期观察、健康评价、遗传疾病预测等的过程。
我们国家的IVD市场起步较晚,但是发展较快,目前正处于快速增长阶段。随着医改的推进和医保范围的进一步覆盖,体外诊断试剂的市场增速会进一步提升。
目前,体外诊断试剂的厂家如雨后春笋般拔地而起,而且从业人员大多高学历,背后又有资本支持,带动了整个医疗器械行业的从业者水平,也加剧了行业之间的竞争。目前,整个行业的政策出台相当密集,对行业从业人员,尤其是注册人员提高了更高的要求,只有不断学习,才能跟上改革步伐。
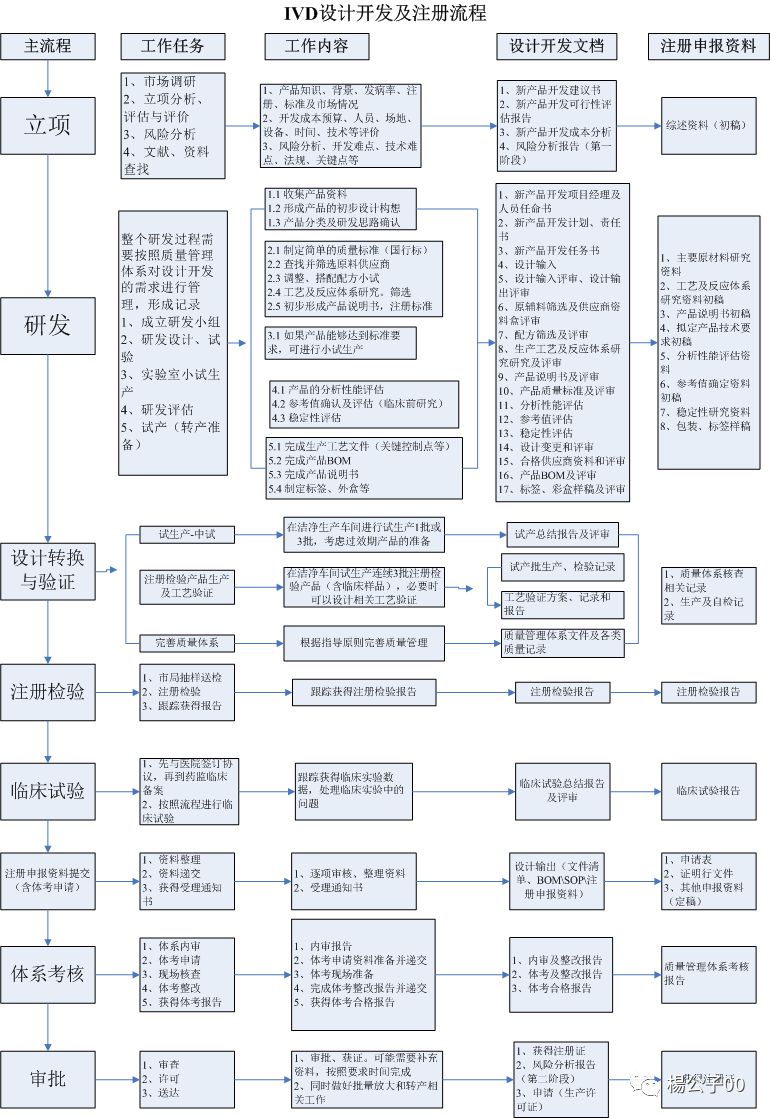
体外诊断包括了机器和试剂两个不可分割的部分。鉴于IVD试剂的注册过程中有很多专门的法律法规,与以往的无菌医疗器械注册有些许不同的地方,笔者专门参照整理了IVD相关的设计开发和注册过程中的资料准备流程图,方便刚入行的同仁快速理清概念,提升效率,节省时间。
|
|
 /3
/3 